国际上疫情再度爆发,对于防疫物质的需求也是与日俱增。近期来咨询口罩出口的企业也非常多,今天我们智皓国际就来谈谈口罩如何是出口以及出口需要的相关资质。
首先我们必须知道您出口的口罩种类。 国内的口罩分三种:
第一种是医用口罩
作为医疗器械管理的医用口罩也分为三种:医用防护口罩、一次性普通医用口罩和医用外科口罩。 生产医用口罩,需要向省级食品药品监督管理局器械处申请办理”医疗器械产品注册证“、”医疗器械生产许可证“。而且还需要10万级以上的洁净车间,并具备微生物试验能力和相关理化试验能力。所谓十万级净化车间就是指空气洁净度为十万级的洁净车间。空气洁净度是指洁净环境中空气含悬浮粒子量的多少的程度,通常空气中含尘浓度高则空气洁净度低,含尘浓度低则空气洁净度高。也就是以每立方米空气中的最大允许粒子数来确定其空气洁净度等级。
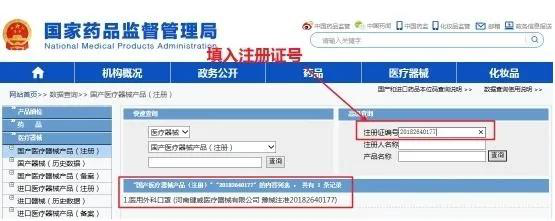
登录“国家药品监督管理局”(www.nmpa.gov.cn)的官网,然后点击“医疗器械”-“国产器械”的栏目。根据页面指示,输入该款口罩的医疗器械注册证号或企业名称等,就可以知道与产品相关的企业生产信息,批准文号信息,即可知道是否合格。
第二种是劳保口罩

劳保口罩也叫 特种劳动防护用品 ,生产此类产品需要向省级技术监督局申请 工业品生产许可证 ,并向国家安全生产监督管理总局申请 “特种劳动防护用品安全标志”认证 ,简称为“LA”认证。
以上两种口罩申报出口时,需要提供以下资料:
1: 营业执照
2:企业生产许可证
3:产品检验报告
4:医疗器械注册证
5:产品说明书、标签
6:产品批次/号
7:产品质量安全书
8:产品样品图片及外包装图片
第三种是日常防护口罩

日常防护口罩相对简单,不用办理任何许可证照,将产品向有资质第三方检测机构按照相应标准送检, 取得国家权威检测报告,具备CMA、CNAS认可标识 ,即可上市销售。
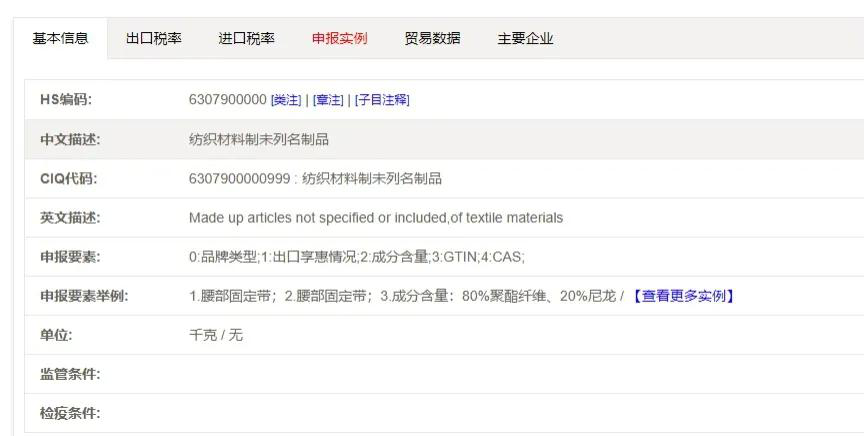
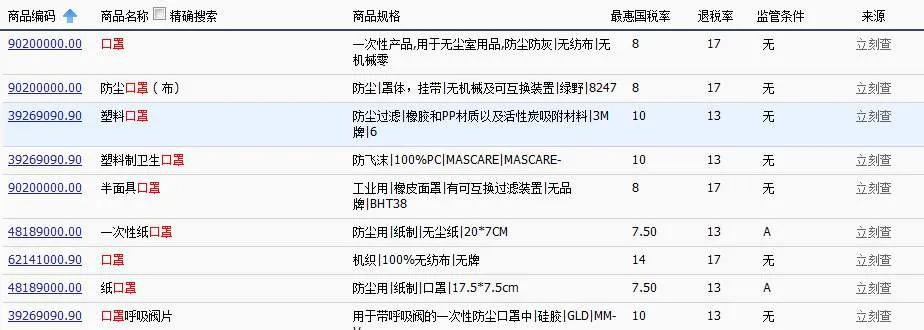
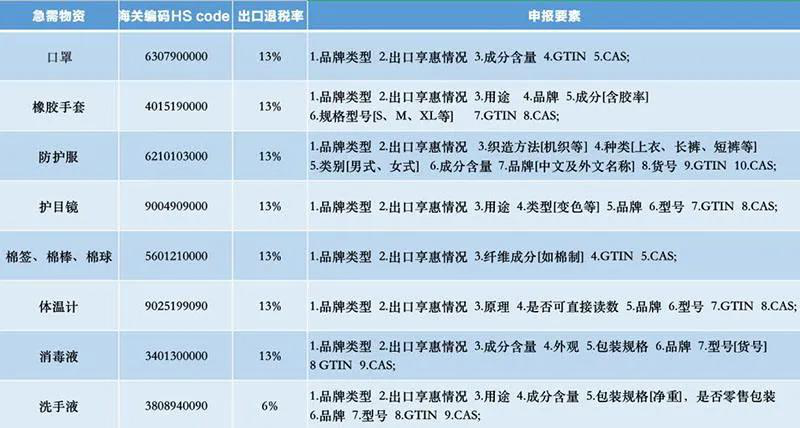
我国海关对口罩出口没有限制,资质齐全的企业和合规的产品可以放心大胆地正常申报,关键是出货以前确认国外的清关要求。 根据《医疗器械监督管理条例(2017修正)》第四十四条:出口医疗器械的企业应当保证其出口的医疗器械符合进口国(地区)的要求。 口罩在不同的国家有不同准入门槛及要求,作为出口企业必须要了解:
如美国对于医用口罩的管理机构是美国食品药品监督管理局(FDA), 出口到美国的口罩若需要销售,必须要拿到美国食品药品监督管理局(FDA)认证 才可以在美国本土市场进行销售活动。在欧盟,口罩属于PPE个人防护用品,“危及健康的物质和混合物”。 根据欧盟新法规,所有出口欧盟的口罩必须获得CE认证证书。 带有CE认证标志的口罩是欧洲经济区批准的用于安全,健康和环保标准的一次性口罩。就像NIOSH根据其效率等级将呼吸器分级为N95,N99或N100一样,CE将其口罩分级为FFP1,FFP2或FFP3。
中国公司口罩出口海外需具备哪些资质?
01、用于销售
需要经营范围内有医疗器械经营许可证的,进出口权的,才能出口。
02、用于赠送或代为采购
作为赠送的,或者代关联公司(兄弟公司,母子公司)采购的,要提供采购的厂家或公司的国内生产厂家的相关资质证明文件,与我们进口时要国外提供三证(营业执照,产品医疗器械备案证明,厂家检查报告)一个道理。
重点国家口罩进口必备资质
美国
01、必要资料(资质)
提单,箱单,发票
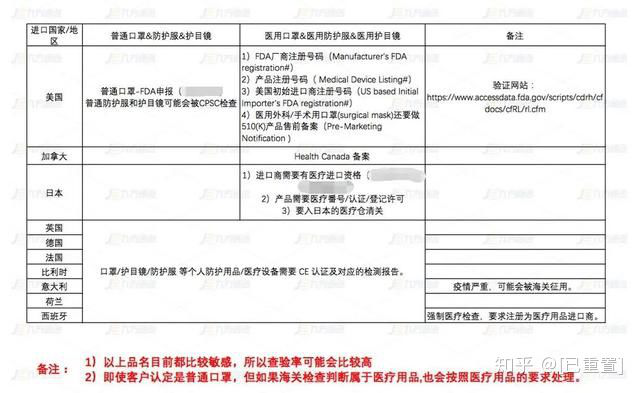
美国进口的口罩,若需要销售,必须要拿到FDA认证才可以在美国本土市场进行销售活动。对于自用和赠送的口罩,大家在出口的时候最好先问一下美国接收方面,是否也需要FDA认证,或者采购原本就通过FDA认证的口罩进行出口。

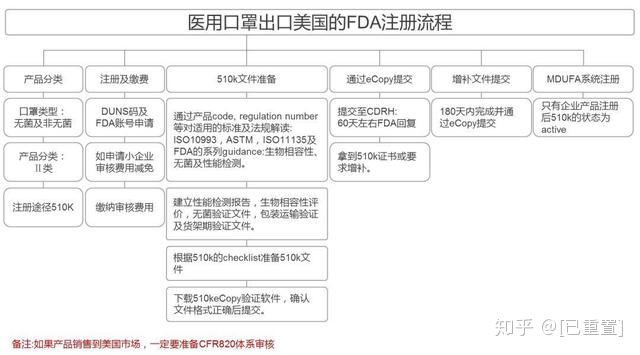
美国口罩分为医用口罩和普通防护口罩。
1.医用口罩出口资质:需要有相关产品的FDA认证(美国食品药品监督管理局)和亚马逊相关产品类目的分类审核,才能上架销售和解决物流清关问题;FDA认证需要每年向美国食品药品监督管理局缴纳一定金额的注册费、年费,收费为5000美元左右。
2.普通防护口罩出口资质:不需要FDA认证,只需要有口罩类目的分类审核就可以销售;另外普通防护口罩的出口需要借助物流商渠道进行FDA申报。
02、口罩要求
根据HHS(美国卫生及公共服务部)法规,NIOSH(美国国家职业安全卫生研究所)将其认证的防颗粒物口罩分为9类。具体的认证则由NIOSH下属的NPPTL实验室操作。
在美国,按过滤网材质的最低过滤效率,可将口罩分为三种等级——N ,R ,P。
N类的口罩只能过滤非油性颗粒物,比如:粉尘、酸雾、漆雾、微生物等。空气污染中的悬浮微粒,也多是非油性的。
R口罩只适合过滤油性颗粒物及非油性颗粒物,但用于油性颗粒物时限制使用时间不得超过8小时。
P类口罩则既可过滤非油性颗粒物,又可过滤油性颗粒物。油性颗粒物比如:油烟、油雾等。
根据过滤效率的不同,又有90,95,100的差别,分别指在标准规定的测试条件下最低过滤效率为90%,95%,99.97%。
N95不是特定的产品名称。只要符合N95标准,并且通过NIOSH审查的产品就可以称为“N95型口罩”。
欧盟
01、必要资料(资质)
提单,箱单,发票
02、口罩要求
在欧盟,口罩属于PPE个人防护用品,“危及健康的物质和混合物”。2019年起,欧盟新法规PPE Regulation (EU) 2016/425强制执行,所有出口欧盟的口罩必须在新法规的要求下获得CE认证证书。

CE认证是欧盟实行的强制性产品安全认证制度,目的是为了保障欧盟国家人民的生命财产安全。
日本
01、必要资料(资质)
提单,箱单,发票。出口日本的PMDA注册医疗器械公司希望把产品投放到日本市场必须要满足日本的Pharmaceutical and Medical Device Act (PMD Act),在PMD Act的要求下,TOROKU注册系统要求国外的制造商必须向PMDA注册制造商信息。
02、口罩要求
包装上印有ウィルスカット99%的字样都是超过国内过滤效率95%(N95口罩)标准的医用口罩!
PFE:0.1um微粒子颗粒过滤效率
BFE:细菌过滤率
VFE:病毒过滤率
ウィルスカット:病毒拦截
00001. 医用防护口罩:符合中国GB 19083-2010 强制性标准,过滤效率≥95%(使用非油性颗粒物测试)。
00002. N95口罩:美国NIOSH认证,非油性颗粒物过滤效率≥95%。
00003. KN95口罩:符合中国GB 2626 强制性标准,非油性颗粒物过滤效率≥95%
注意:需要供应商具备二类医疗器械经验许可凭证,产品需要医疗番号/认证/登记许可证,且还需要入日本的医疗仓清关,情况特殊复杂,建议卖家谨慎考虑。
韩国
01、必要资料(资质)
提单,箱单,发票,韩国进口商营业执照,韩国收货人需要到韩国药监局Korea Pharmaceutical Traders Association. 提前备案进口资质(没有不行)。
网址:www.kpta.or.kr
企业自用又是受赠的情况,可以自行进口,不需要有相关资质。
02、口罩要求
韩国的口罩标准KF (Korean filter) 系列,KF系列标准是由韩国的食品药品管理部门发布的韩国主流口罩标准 。KF系列分为KF80、KF94、KF99。KF80:≥80% (仅盐性介质) ;KF94:≥94%(油性和盐性介质) ;KF99:≥99% (油性和盐性介质) 。
口罩还需要有详细的原产地标识,如果是中国制造务必有标签:Made in China, 生产厂家信息、保质期,还要准备成分含量说明,制造工艺流程,这些文件都有了还没有结束,还需要货物到了韩国以后进行精监化验送交样品到实验室,化验合格后方可进入韩国市场销售流通。
澳大利亚
01、必要资料(资质)
提单,箱单,发票
02、口罩要求
AS/NZS 1716:2012是澳大利亚和新西兰的呼吸保护装置标准,相关产品制造流程和测试必须符合本规范。
该标准规定了防颗粒口罩制造过程中必须使用的程序和材料,以及确定的测试和性能结果,以确保其使用安全。
03、个人行邮方式
00001. 由于每个国家关于进口口罩的要求不同,建议大家出口前务必咨询当地的代理公司或者接收方,避免物资被扣或者被退回的问题。
00002. 自用口罩的出口以及快递,数量一定要在合理范围,如果数量巨大也有可能被国外海关扣押。
00003. 目前航空海运运力部分暂停,运输时间都相对较长,建议在发货后留意单号更新,同时耐心等待,只要没有违规问题,一般不会被扣押或者退回。
再次提醒:
建议中国卖家及时关注国内外防疫物资出口资质认证和监管要求,避免造成产品被扣押和退回的风险。属于医疗器械类的口罩,不同国家的资质和要求都不相同,这点卖家们一定要注意。国内外销售都需要先获得《第二类医疗器械经营备案凭证》,若想在跨境平台销售,除了类目审核,还需要产品认证,欧美必须通过当地国家认证许可,如欧盟CE认证,美国NIOSH认证。欧盟CE认证还需要注意包装、质量符合要求,要有欧洲代理信息。并最好保留好认证证书,采购发票或原材料发票。
没有一个冬天不可逾越,没有一个春天不会到来,春暖花开始,山河定无恙!愿早日战胜疫情。 心有大我,至诚报国。祝愿早日战胜疫情,明媚的阳光终会照亮这片土地。 愿我们早日能战胜疫情,摘下口罩去想去的地方,见想见的人。



